商機詳情 -
蘇州NDAeCTD軟件
eCTD的法規框架與技術規范:歐盟eCTD的法規層級包括指南(Guidelines)、指令(Directive)和法規(Regulation)。其中,法規(如CTR)具有直接法律效力,而指南(如ICH eCTD規范)則為技術操作提供參考。eCTD的結構需符合歐盟模塊1規范(DTD 3.0+),包含行政文件(模塊1)、質量數據(模塊3)及臨床研究報告(模塊5)等內容,并通過XML文件實現數據互聯。例如,CEP(歐洲藥典適用性證書)的eCTD申報需單獨構建信封(Envelope)和模塊1,并指定標識符(UUID)以確保技術合規性。加拿大NDA注冊申報相關技術支持。蘇州NDAeCTD軟件
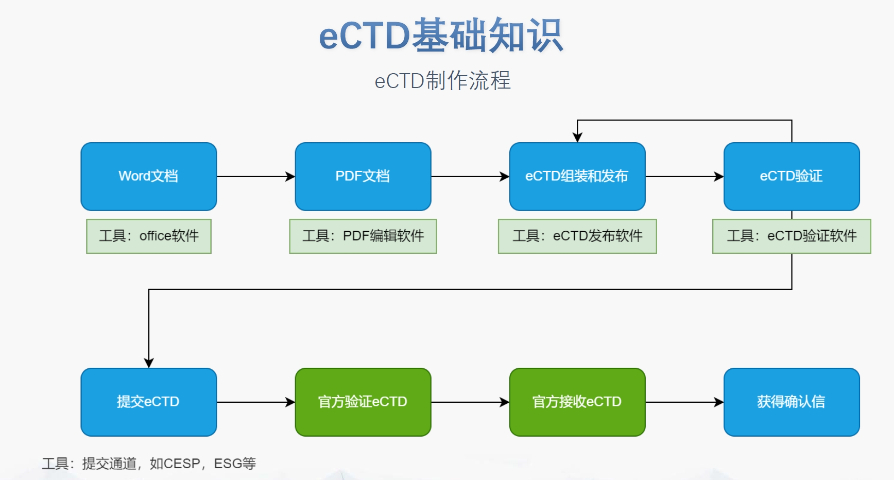
多國審評程序與eCTD遞交途徑的適配:歐盟藥品審評程序包括集中(CP)、分散(DCP)、互認(MRP)和國家程序(NP),eCTD需適配不同程序的遞交要求。例如: ?集中審評程序(CP)?:通過EMA的eSubmission Gateway提交,審評時限約240個工作日,eCTD需包含完整的模塊1-5及多語言標簽文件。 ?分散審評程序(DCP)?:需通過CESP(歐盟共同提交門戶)遞交,參考成員國(RMS)主導審評,eCTD需支持多國同步評估的模塊化拆分。 ?互認程序(MRP)?:已授權成員國作為RMS,eCTD需包含基線序列(Baseline Sequence 0000)以整合歷史審評數據,并通過CMDh協調分歧。太倉原料藥eCTD哪家好瑞士eCTD注冊申報相關技術支持。

eCTD在歐盟藥品監管中的歷史背景:歐盟eCTD(電子通用技術文檔)的發展始于對臨床試驗和藥品審評流程標準化的需求。2001年,歐盟引入《臨床試驗指令》(CTD)作為統一的法律框架,但其分散的成員國申報機制導致效率低下。2014年,歐盟通過《臨床試驗法規》(CTR, Regulation EU No. 536/2014),要求通過CTIS平臺(臨床試驗信息系統)集中提交臨床試驗申請(CTA),并逐步推動eCTD作為電子化申報的工具。這一旨在解決傳統CTD模式下審評周期長、多國協調成本高的問題,為eCTD的實施奠定了基礎。
賦悅Word插件 自主研發Word插件 快速編輯:整合word常用功能按鈕,避免頻繁切換菜單;內置標題、段落、文字、目錄、超鏈接等的格式和樣式,可快速設置和更文檔的格式 快速鏈接:雙擊或者拖拽的方式,制作文本超鏈接或者題注超鏈接;可搜索全文關鍵字,自動制作超鏈接 文檔拆分:可根據不同的條件將word文件顆粒化,如分節符、頁眉、頁腳、頁碼范圍和自定義頁碼等 PDF轉換:WORD轉PDF,自動判斷是否生成書簽,自動鑲嵌所有字體,生成PDF快速網頁瀏覽的PDF,確保生成的PDF所有屬性符合法規要求 文檔驗證:驗證文檔的字體、字號、紙張、頁面布局、空白頁、頁碼、編號、目錄、超鏈接等,并且可以定位驗證結果 可定制:可根據用戶需求定制格式和樣式模板澳大利亞ANDA注冊申報相關技術支持。
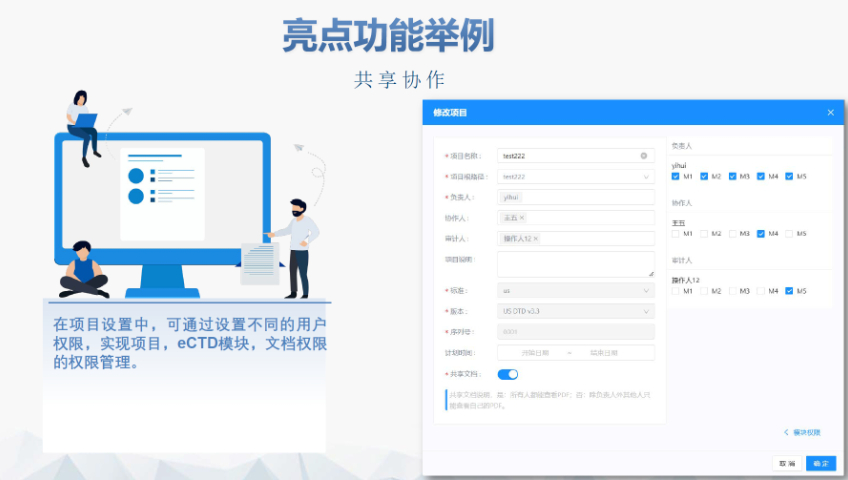
賦悅eCTD系統 ?文件驗證與修復 支持自動驗證文件格式(如PDF屬性、字體嵌入、超鏈接完整性等),并一鍵修復不符合法規要求的文件。例如,系統會自動檢查XML主干文件的結構合規性,確保符合中國、美國、歐盟等地區的eCTD法規標準。 ?eCTD組裝與發布 可自動生成符合CTD結構的電子文檔包,包括XML主干文件、文件夾命名規范及序列號管理(如申請號/序列號文件夾自動生成),并支持超鏈接和書簽的批量創建。例如,初次提交的序列號為0000,后續每次提交自動遞增。 ?生命周期管理 支持文件全生命周期操作(增、增補、替換、刪除),并通過序列號疊加直觀顯示各章節文件的有效性,覆蓋從初次提交到年報、撤市的全流程管理。 ?協同與權限管理 基于B/S架構(瀏覽器/服務器),支持云端或本地靈活部署,全集團賬號通用。提供多用戶協作功能,包括權限分級、審計追蹤、文件版本控制等。 ?法規支持與專業服務 內置符合中國CDE、美國FDA、歐盟EMA等法規的模板,同時提供注冊咨詢、資料撰寫、eCTD格式代轉等全流程支持,團隊擁有17年藥品注冊經驗。歐盟ANDA注冊申報相關技術支持。工業園區賦悅科技eCTD文件如何制作
eCTD申報軟件相關技術支持。蘇州NDAeCTD軟件
2020年暴發后,FDA進一步推動電子化進程,例如允許遠程電子簽章和臨時放寬部分格式要求,但驗證標準(如PDF版本、書簽鏈接有效性)并未降低。這一時期的實踐為eCTD在緊急審批中的靈活性提供了案例,也凸顯了其作為危機應對工具的價值。 盡管美國尚未部署eCTD V4.0,但其技術方向已明確:支持醫療器械和保健品申報、增強數據可復用性、優化審評系統與人工智能的集成。此外,區塊鏈技術在電子簽章和數據溯源中的應用探索,可能成為下一階段升級的重點蘇州NDAeCTD軟件