商機詳情 -
無錫原料藥eCTD服務電話
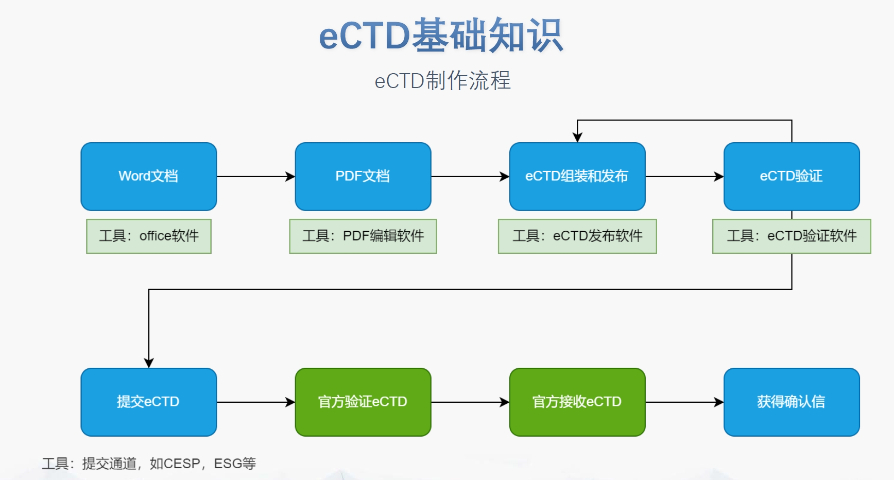
電子遞交的合規性與風險管理 歐盟要求申請人確保電子資料與紙質版本完全一致,若未在規定時間提交紙質文件可能導致注冊終止。驗證過程中,“錯誤”級別問題(如文件命名不規范、XML邏輯錯誤)必須修正,而“警告”和“提示信息”則建議優化以提升審評體驗。EDQM和EMA均提供驗證工具,申請人需在遞交前完成內部預驗證。 官方費用結構與支付流程 歐盟eCTD遞交費用因審評程序類型而異:集中程序費用較高,涵蓋科學評估和合規審查成本;國家程序費用由各成員國自行設定。CEP申請需向EDQM支付評審費,具體金額根據原料藥類型和變更復雜度分級。繳費需通過官方指定渠道完成,并附上付款憑證作為模塊1的組成部分。 多語言支持與翻譯要求 盡管歐盟允許使用英語提交,但部分成員國要求模塊一的行政文件翻譯為本地語言。臨床試驗數據庫(如SDTM和ADaM)需以英語呈現,同時提供雙語標簽以支持多國審閱。專業翻譯服務在確保技術術語準確性方面至關重要,尤其針對復雜藥學和非臨床數據。美國eCTD注冊咨詢相關技術支持。無錫原料藥eCTD服務電話
電子簽章與傳輸安全 文件需經AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗碼。光盤損壞或病毒污染將觸發重遞交流程,原載體按銷毀程序處理。 ?審評與核查協同 自2018年起,FDA要求提交兩套光盤分別用于審評和現場核查,2022年調整為“1套審評+1套核查+1套專項資料”模式,提升流程效率。 ?國際化兼容性增強 美國eCTD系統支持與歐盟、日本等地區的XML互操作性,但區域差異(如模塊1的標簽要求)仍需人工適配。 ?未來通道創 FDA計劃引入API接口支持企業系統直連,并探索基于云存儲的實時提交與審評,減少物理媒介依賴。閔行區中國eCTD找哪家美國eCTD驗證標準相關技術支持。
GDUFA III框架與費用分類 2022年更的GDUFA III將費用分為ANDA申請費、DMF認證費、項目費及設施費四類,實施周期至2027年。2025財年ANDA費用漲至約22萬美元,較2024年增幅達27.5%,反映審評成本上升。 ?ANDA申請費規則 費用需在提交時繳納,若申請被拒可退還75%。重提交視為申請,需再次繳費。關聯API的工廠數量影響總費用,例如某ANDA引用3個API且涉及6家工廠,需支付6倍DMF費用。 ?DMF費用機制 II類原料藥DMF需在引用前繳費,一次性支付約5.3萬美元(2025財年)。未繳費DMF不得用于支持ANDA,否則觸發退審。 ?項目費分級管理 根據企業獲批ANDA數量分為大、中、小型三級,2025年大型企業年費約34萬美元。附屬公司ANDA數量合并計算,繳費責任可由母公司或任一附屬公司承擔。
ANDA一般不需要提供臨床前(動物)和臨床(人體)數據來證明其安全性和youxiao性(即免毒理和臨床),作為替代,申請人必須合理證明其產品與原研YAO相比是shengwu等效的。按照《聯邦食品、YAO品和化妝品法》第505(j)章要求,擬向FDA遞交申請ANDA的YAO品需符合以下條件:仿制YAO必須依照FDA《經過yiliao等同性評價批準的YAO品》(俗稱"橙皮書")上所列,由FDA選定的RLD/RS進行對照仿制;活性成份、劑型、規格、給YAO途徑、適應癥,要與RLD相同;仿制YAO必須證明與RLD在shengwu效果上等同,即具有shengwu等效性;必須按照美國聯邦管理法21CFR遵行YAO品生產管理規范kongzhi生產過程;無論CN還是美國,要求仿制YAO的質量必須等同或者是高于參比制劑的,這是獲批的基本要點;注意:如果原研YAO未被列為RLD,申請人可以提出公民,向FDA申請。eCTD注冊咨詢相關技術支持。
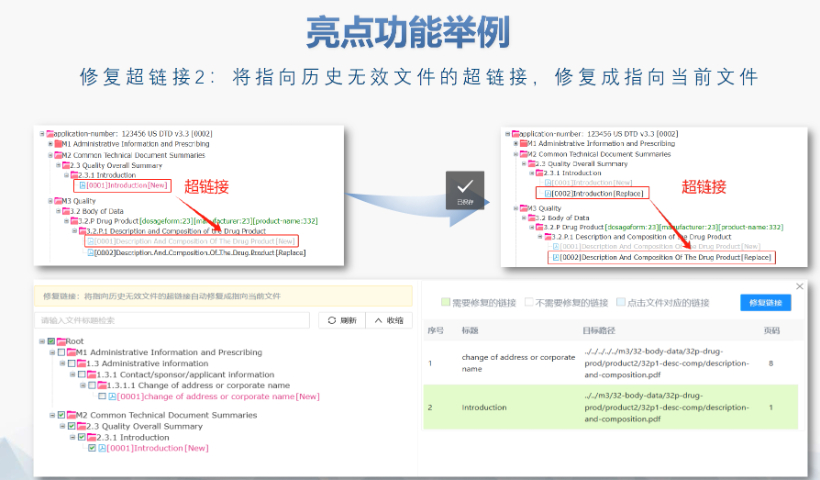
電子簽章與安全性 FDA要求所有PDF文件需經數字簽名,并通過MD5校驗確保傳輸完整性。簽章需符合21 CFR Part 11的電子記錄規范,部分情況下允許臨時放寬(如期間的遠程簽署)。 ?多模塊協同驗證 模塊1(行政文件)的區域性元數據(如申請類型、聯系人信息)需與模塊2-5的內容邏輯一致。例如,生物制品的3.2.R擴展節點命名需遵循特定規則,而化學藥品則禁止使用此類擴展。 ?驗證工具與流程 主流工具如LORENZ eValidator支持自動化驗證,生成包含錯誤定位與修復建議的詳細報告。企業需在提交前完成內部驗證,并通過“藥品業務應用系統”推送受理狀態。 ?常見問題與規避策略 高頻錯誤包括PDF安全設置、書簽鏈接失效、STF(研究標簽文件)缺失等。例如,未在5.3.1章節標注研究ID會導致驗證警告,需通過說明函解釋。企業可通過建立標準化模板庫和預檢流程降低風險。 ?后續監管與更 FDA定期更驗證標準(如2022年增臨床試驗數據完整性檢查),企業需通過訂閱官方通知或第三方服務商獲取動態加拿大eCTD驗證標準相關技術支持。上海生物制品eCTD醫療科技
澳大利亞eCTD驗證標準相關技術支持。無錫原料藥eCTD服務電話
eCTD的實施為監管機構和企業帶來了多重機遇。電子化申報資料能夠極大地加速審評效率,減少人為判斷錯誤和數據混淆的情況,從而提高審評的準確性和速度。同時,eCTD帶來的數據標準化機遇使得全球監管機構的資料內容和電子格式得以統一,有助于在不同監管機構之間進行數據傳輸和共享。這對于提升全球監管效率和行業研發效率具有重要意義。此外,eCTD的實施還促進了全球合作,構建了全球監管的底層大數據基礎。對于企業而言,eCTD提供了一個規范化的研發活動模板,有助于降低與監管機構溝通的成本,提高申報效率。特別是對于國內的醫技術企業而言,eCTD的實施更是具有重要意義,有助于這些企業更好地走向全球市場。然而,中小企業在享受這些機遇的同時,也面臨著技術和成本壓力。eCTD的實施需要專門的團隊進行系統維護和開發,這對于中小企業來說是一筆不小的開支。同時,數據安全問題也是企業關注的焦點。此次CDE擴大eCTD實施范圍對行業而言是一個積極的風向標。短期內,企業面臨的挑戰包括適應更高要求的技術規范并提高文件質量、和eCTD出版系統的磨合以及進行eCTD知識的跨職能培訓等。 無錫原料藥eCTD服務電話