商機詳情 -
浙江eCTD
歐盟eCTD的歷史沿革與強制實施 歐盟自2003年逐步推進eCTD(電子通用技術文檔)的標準化進程,初要求藥注冊申請(MAA)采用CTD格式。2010年,集中審評程序(CP)率先強制使用eCTD,隨后分散程序(DCP)和互認程序(MRP)分別于2015年、2017年跟進。至2019年,歐盟要求所有國家程序(NP)的注冊申請均以eCTD格式提交,標志著其電子遞交體系的成熟。2024年,EMA啟動eCTD4.0試點項目,旨在提升技術兼容性與審評效率。 eCTD驗證標準的迭代與關鍵更 歐盟的驗證標準歷經多次調整,例如2025年3月啟用的eCTD3.1區域模板和驗證規則v8.1,對文件結構、元數據和內容完整性提出更嚴格的要求。標準引入的“追蹤表(Tracking Table)”強制校驗規則(如15.11和15.12)曾導致CEP(歐洲藥典適用性證書)遞交,后通過允許占位文件臨時解決。與早期版本相比,v8.1強化了對模塊一區域信息的邏輯驗證,并細化了對PDF書簽、超鏈接的規范性檢查。加拿大eCTD注冊外包相關技術支持。浙江eCTD
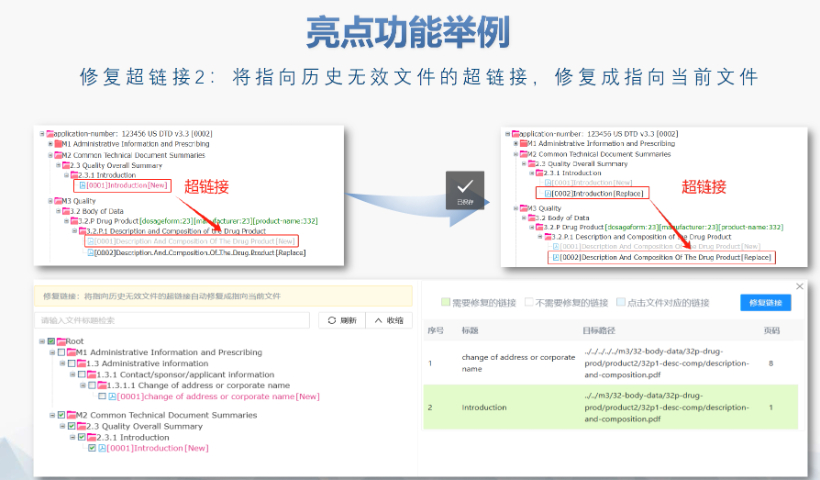
美國eCTD驗證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正)、“提示信息”(參考)。例如,PDF文件版本不符或加密保護屬于“錯誤”,而書簽路徑非相對性則可能列為“警告”。驗證失敗將直接導致退審,企業需通過LORENZ Validator等工具預檢,確保提交前合規。 ?技術驗證點 驗證涵蓋XML結構合規性、文件命名規則、生命周期管理(如序列號連續性)及PDF屬性(如字體嵌入、可搜索性)。臨床試驗數據需額外滿足CDISC標準,包括SDTM和ADaM數據集的結構驗證工業園區CDE eCTD發布軟件瑞士eCTD注冊外包相關技術支持。

申報流程與要求 ?資料準備 ?內容要求:包括產品描述、生產工藝(原材料來源、設備參數等)、質量控制標準(SOP、穩定性數據)、安全性與毒性研究等。 ?格式規范: 采用CTD(通用技術文件)格式,按模塊分章節(如模塊3為CMC數據)。 電子提交需符合eCTD標準(文件小于10GB通過ESG系統提交,超過可選用CD-ROM)。 ?提交與注冊 ?預分配DMF號:需在提交前申請,確保文件與編號綁定。 ?授權書(LOA)?:需向引用DMF的制劑廠商提供授權信,明確可查閱的章節。 ?費用:Ⅱ類原料藥DMF需繳納年費(2024年約9,468美元)。 ?FDA審核流程 ?行政審評:2-3周內確認文件完整性。 ?完整性審評(CA)?:針對Ⅱ類DMF,約60天。 ?技術審評:在DMF被制劑申請(如ANDA、NDA)引用時啟動,周期60-180天。 ?結果反饋:FDA可能要求補充數據,但DMF本身無“批準”狀態,通過后可能收到“無進一步意見函”(No Further Comment Letter)。
eCTD驗證標準的嚴格性與分類:歐盟對eCTD的驗證要求分為“錯誤”“警告”和“提示信息”三級,其中“錯誤”項直接導致申報被拒。驗證項目涵蓋六大類共149條,包括文件命名規范(如路徑長度限制)、PDF可讀性(禁止密碼保護)、XML骨架文件完整性等。例如,文件擴展名必須符合規范(如.xpt用于臨床數據集),而文件夾層級需避免空目錄或混合存放文件。相較于中國《電子申報驗證標準》的簡化版(54條),歐盟的驗證體系更為復雜,體現了其高標準的技術監管。美國注冊鄧白氏號申請相關技術支持。
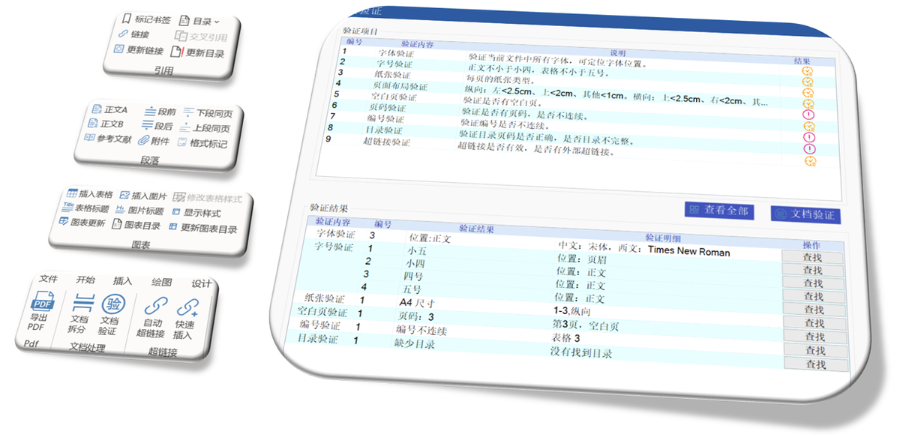
ANDA一般不需要提供臨床前(動物)和臨床(人體)數據來證明其安全性和有效性(即免毒理和臨床),作為替代,申請人必須合理證明其產品與原研藥相比是生物等效的。 按照《聯邦食品、藥品和化妝品法》第 505(j)章要求,擬向FDA遞交申請ANDA的藥品需符合以下條件: 仿制藥必須依照FDA《經過醫療等同性評價批準的藥品》(俗稱"橙皮書")上所列,由FDA選定的RLD/RS進行對照仿制; 活性成份、劑型、規格、給藥途徑、適應癥,要與RLD相同; 仿制藥必須證明與RLD在生物效果上等同,即具有生物等效性; 必須按照美國聯邦管理法21 CFR遵行藥品生產管理規范控制生產過程; 無論中國還是美國,要求仿制藥的質量必須等同或者是高于參比制劑的,這是獲批的基本要點; 注意:如果原研藥未被列為RLD,申請人可以提出公民,向FDA申請。美國eCTD驗證標準相關技術支持。寧波生物制品eCTD文件如何制作
美國eCTD注冊外包相關技術支持。浙江eCTD
eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,包括提交、補充申請及實質性變更。例如,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產工藝調整)需創建序列并通過CTIS平臺更模塊3和模塊1的GMP證明。技術驗證工具(如EDQM推薦的檢查軟件)需在每次提交前運行,確保XML骨架文件與PDF書簽層級符合規范。此外,電子簽章需符合《歐盟電子簽名法》,并在模塊1中明確標注法律效力。歐洲通用提交門戶(Common European Submission Portal,CESP)是歐盟及成員國藥品監管機構間用于電子化提交申報資料的重要平臺。以下是關于CESP的詳細介紹: CESP是由歐盟藥品監管部門負責人網絡(HMA)合作開發的在線交付系統,旨在為藥品注冊申請者、利益相關方和監管機構之間提供統一、安全的電子提交通道。其設計初衷是簡化跨國申報流程,允許通過單一門戶向多個歐洲國家的藥監部門同時提交申請,避免了重復操作。浙江eCTD
賦悅科技(杭州)有限責任公司匯集了大量的優秀人才,集企業奇思,創經濟奇跡,一群有夢想有朝氣的團隊不斷在前進的道路上開創新天地,繪畫新藍圖,在浙江省等地區的數碼、電腦中始終保持良好的信譽,信奉著“爭取每一個客戶不容易,失去每一個用戶很簡單”的理念,市場是企業的方向,質量是企業的生命,在公司有效方針的領導下,全體上下,團結一致,共同進退,**協力把各方面工作做得更好,努力開創工作的新局面,公司的新高度,未來賦悅科技供應和您一起奔向更美好的未來,即使現在有一點小小的成績,也不足以驕傲,過去的種種都已成為昨日我們只有總結經驗,才能繼續上路,讓我們一起點燃新的希望,放飛新的夢想!