商機詳情 -
深圳偏光成像紡錘體胚胎植入
卵母細胞冷凍保存主要采用兩種方法:慢速冷凍法和玻璃化冷凍法。相較于傳統的慢速冷凍法,玻璃化冷凍法因其更高的解凍存活率和妊娠成功率而逐漸成為主流技術。玻璃化冷凍法的基本原理是將含有生物樣本的溶液在極短的時間內(如幾分鐘內)冷卻至液氮溫度,使溶液在凝固點以下形成無冰晶的半固體或固體狀態。這種方法避免了冰晶形成對細胞結構的破壞,從而減少了冷凍損傷。在卵母細胞冷凍保存中,玻璃化冷凍法通過優化冷凍保護劑的濃度和冷凍速率,使卵母細胞在冷凍過程中保持其結構的完整性。紡錘體的微管從中心體向外輻射,形成紡錘狀結構。深圳偏光成像紡錘體胚胎植入
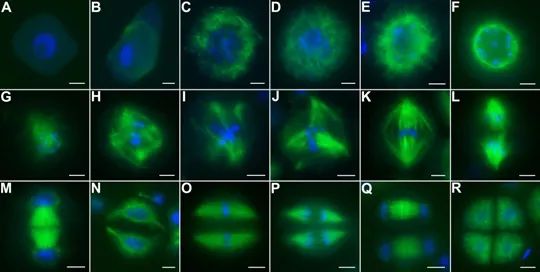
在生殖醫學領域,卵母細胞冷凍保存技術作為輔助生殖技術的重要組成部分,近年來取得了進展。尤其是針對成熟卵母細胞紡錘體的冷凍保存研究,不僅關乎女性生育能力的保存,還涉及到遺傳學的穩定性和安全性。成熟卵母細胞,即處于第二次減數分裂中期(MII期)的卵母細胞,其內部包含一個高度復雜且精細的紡錘體結構。紡錘體由微管組成,這些微管通過動態變化,將染色體緊密地聯系在一起,并確保在細胞分裂過程中染色體的正確分離。成熟卵母細胞的紡錘體對溫度變化和機械刺激極為敏感,這使得其冷凍保存過程充滿了挑戰。香港無損觀察紡錘體價格紡錘體的主要功能是在細胞分裂時牽引染色體分離,確保遺傳信息的正確傳遞。
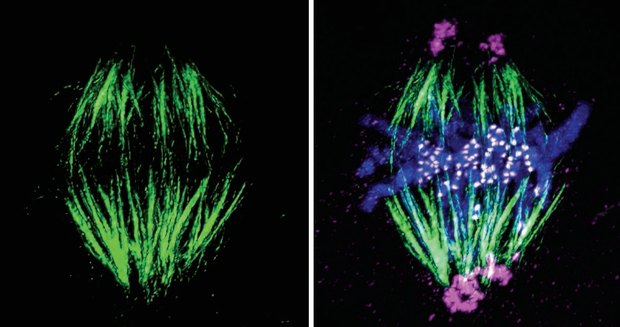
紡錘體是卵母細胞在減數分裂過程中形成的一種微管結構,負責精確分離染色體。然而,紡錘體對環境溫度、滲透壓等外部條件極為敏感,在冷凍保存過程中容易發生損傷,導致染色體分離異常,進而影響卵母細胞的發育潛力和受精后的胚胎質量。因此,如何有效監測和評估冷凍過程中紡錘體的變化,成為紡錘體卵冷凍研究的重要課題。紡錘體實時成像技術的出現,為這一問題的解決提供了可能。紡錘體實時成像技術主要利用高分辨率顯微鏡結合熒光標記技術,對卵母細胞內的紡錘體進行實時、動態的觀察和記錄。常用的熒光標記方法包括使用綠色熒光蛋白(GFP)標記微管蛋白,以及利用特定抗體對紡錘體相關蛋白進行染色。通過這些方法,研究者可以清晰地觀察到紡錘體的形態、位置、動態變化等信息,從而準確評估冷凍過程中紡錘體的穩定性和完整性。
紡錘體檢查點是確保染色體正確分離的重要機制,其失效會導致染色體分離錯誤。例如,某些基因突變(如MAD2突變)會影響SAC的功能,導致染色體非整倍性的發生。SAC信號傳導異常:SAC通過復雜的信號傳導途徑確保染色體的正確分離。SAC信號傳導異常會導致紡錘體檢查點失效,增加染色體非整倍性的風險。染色體在分裂過程中未能正確分離,導致非整倍體的形成。例如,某些基因突變(如CENP-A突變)會影響染色體的正確分離,導致染色體非整倍性的發生。染色體橋是染色體在分裂過程中未能完全分離形成的結構,會導致染色體非整倍性的發生。例如,某些基因突變(如PLK1突變)會影響染色體橋的形成。紡錘體在細胞分裂中扮演關鍵角色,確保遺傳物質均等分配。
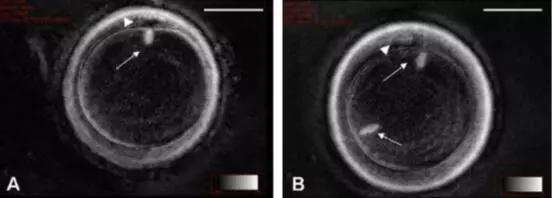
玻璃化冷凍技術因其快速冷凍和解凍的特點,在哺乳動物紡錘體卵冷凍保存中展現出巨大優勢。該技術通過極快的降溫速率和高濃度的冷凍保護劑,使細胞內溶液在冷凍過程中呈玻璃態而非結晶態,從而避免了冰晶對紡錘體的損傷。此外,研究者們還嘗試將微流控技術、激光輔助冷凍等新技術應用于卵母細胞的冷凍保存中,以進一步提高冷凍效果。為了準確評估冷凍對紡錘體的影響,研究者們開發了多種紡錘體穩定性評估技術。例如,通過偏光顯微鏡觀察紡錘體的形態變化;利用免疫熒光染色技術檢測紡錘體相關蛋白的分布和表達;以及通過分子生物學方法檢測紡錘體相關基因的轉錄和翻譯水平等。這些技術的應用為深入研究冷凍過程中紡錘體的變化提供了有力支持。紡錘體的異常也是疾病發生和發展的一個重要因素。深圳紡錘體觀測儀
紡錘體微管的數量和分布隨細胞分裂階段而變化。深圳偏光成像紡錘體胚胎植入
細胞生物學領域,紡錘體作為有絲分裂過程中的主要結構,發揮著至關重要的作用。它不僅確保了染色體的精確分離,還決定了胞質分裂的分裂面,從而保證了遺傳信息的穩定傳遞和細胞增殖的準確性。紡錘體是一種在細胞分裂前期形成的臨時性細胞器,由微管、微管結合蛋白以及多種調節蛋白組成。微管是紡錘體的主干,由α、β微管蛋白異源二聚體及少量微管結合蛋白聚合而成,呈現出動態生長和縮短的特性。在動物細胞中,紡錘體由星體微管、極間微管和動粒微管構成,這些微管在中心體的引導下,從兩極向中心區域延伸,形成一個類似紡錘的形狀。而在植物細胞中,紡錘體則是由細胞兩極發出的紡錘絲直接構成,不含有星體微管,因此被稱為無星紡錘體。 深圳偏光成像紡錘體胚胎植入