商機詳情 -
湖南菌群移植怎么做
近年來,隨著人口老齡化進程不斷加快,人民慢性病疾病負擔日益沉重,成為影響國家經濟社會發展的重大公共衛生問題。例如,我國的constipation患者超過2億;我國IBD患者近十年的發病人數達到前面十年的2.5倍,目前預計約有150萬患者;我國消化道疾病特別是Colorectalcancer呈現快速增加的趨勢,每年Colorectalcancer的發病人數達到37.6萬人,且仍在以4.2%的速度快速增長;我國自閉癥現存人群約有1000萬;我國抑郁癥人群近6000萬;我國超重和肥胖患者達到3億人,其中肥胖患者超過9000萬。目前的研究發現腸道菌群與慢性疾病之間存在緊密聯系,菌群移植可以通過人為調節人體腸道微生物達到緩解疾病的目的,極具臨床應用前景!在進行菌群移植前,需要對供體進行嚴格的篩選,確保其腸道菌群健康且無傳染性疾病。湖南菌群移植怎么做

菌群移植移植途徑的選擇:推薦在行FMT前評估消化道動力(1D)消化道動力影響菌液在消化道中的停留時間。另一方面,對于消化道動力差的患者,如一次性輸注過多菌液,則極有可能引起或加重惡心、嘔吐、腹脹、肚子疼等不良反應,故在行FMT前需評估消化道動力,并作為確定FMT路徑與單次輸注菌液體積的參考。例如,存在胃排空障礙的患者,不宜采用口服或鼻胃管路徑;腸道動力緩慢的患者,應適當減少一次性輸注菌液的量或減慢輸注速度。消化道動力評估首先應詢問病史,對于明顯存在腸道動力紊亂的患者,可采用口服鋇劑或小腸插管碘水造影法,既能動態觀察消化道蠕動狀況、又能觀察消化道有無形態結構異常。不建議進行結腸傳輸試驗,因為它耗時久、且不利于動態觀察,意義不大.陜西腸道菌群移植是什么意思探索健康新奧秘,上海沃本菌群移植,為您的腸道健康保駕護航。

菌群移植臨床改善或緩解標準:5.腸易激綜合征(IBS):連續3個月未出現與排糞頻率、排糞形式相關的肚子痛或不適癥狀,且菌群多樣性恢復至供體菌群多樣性50%以上為改善。滿足下列任1條即為顯效:(1)診療開始后連續1周未出現肚子痛或不適.(2)IBS?C患者排硬或塊狀糞便<25%、同時稀或水樣糞便<25%,IBS?D患者排稀或水樣糞便<25%、同時硬或塊狀糞便<25%,IBS?M患者排硬或塊狀糞便<25%、同時稀或水樣糞便<25%(1C)6.自閉癥:診療第12周,自閉癥ABC量表評分<31分、且CGI?I評分1分,菌群多樣性恢復至供體菌群多樣性50%以上為診療顯效。診療第12周自閉癥ABC量表評分<67分、且CGI?I評分1~2分或5個ABC子量表中至少2個較基線有50%或更大的下降,而其他子量表均未出現10%或更大的上升為診療有效(2C).
菌群移植移植途徑的選擇:推薦在行FMT前評估消化道動力(1D)消化道動力影響菌液在消化道中的停留時間。另一方面,對于消化道動力差的患者,如一次性輸注過多菌液,則極有可能引起或加重惡心、嘔吐、腹脹、肚子疼等不良反應,故在行FMT前需評估消化道動力,并作為確定FMT路徑與單次輸注菌液體積的參考。例如,存在胃排空障礙的患者,不宜采用口服或鼻胃管路徑;腸道動力緩慢的患者,應適當減少一次性輸注菌液的量或減慢輸注速度。消化道動力評估首先應詢問病史,對于明顯存在腸道動力紊亂的患者,可采用口服鋇劑或小腸插管碘水造影法,既能動態觀察消化道蠕動狀況、又能觀察消化道有無形態結構異常。不建議進行結腸傳輸試驗,因為它耗時久、且不利于動態觀察,意義不大!菌群移植前需進行嚴格篩選與匹配,確保移植菌群的安全性與有效性。
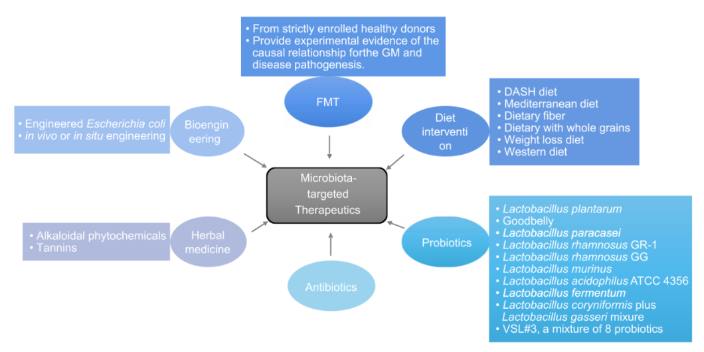
菌群移植(Fecalmicrobiotatransplantation,FMT)當時被用于改善rCDI,有效率超過90%,目前已被臨床醫學指南及共識推薦用于復發性或難治性CDI,并逐漸推廣應用于慢性constipati、腹瀉、腸易激綜合征(Irritablebowelsyndrome,IBS)和炎性腸病(Inflammatoryboweldisease,IBD)等腸道功能性和器質病變以及神經精神系統(自閉癥、焦慮、抑郁癥和帕金森病)、代謝系統和tumour免疫診療等。以上疾病病因復雜且傳統的藥物診療效果非常有限,應用FMT技術診療卻獲得了大部分的療效認可。FMT診療constipati患者的變好率較常規診療可提高3倍以上;IBD可以獲得較長時間的臨床完全緩解,特別是針對年輕的IBD患者以及克羅恩病患者,FMT的緩解率超過60%;糞便菌群移植2年后,自閉癥癥狀減輕了近50%。FMT診療是一種創新的、具有明確臨床意義的診療方案,甚至被認為是新療法!通過菌群移植,科學家成功治好了部分患者的慢性腸道疾病。河北腸道菌群移植多久見效
菌群移植的方式主要有結腸鏡、灌腸和口服膠囊等。湖南菌群移植怎么做
本研究通過小鼠模型揭示了人類炎癥性腸病(IBD)患者的腸道微生物群移植(FMT)效率是實驗變異性的一個重要來源,而適應于小鼠環境的人類IBD患者腸道微生物群則能高效穩定地轉移,導致更為一致和可重復的結腸炎表型;2直接從人類轉移到小鼠的FMT導致了微生物群組成的高度個體間變異,而經過小鼠適應的FMT則顯示出低變異性和高一致性;3小鼠適應過程中的炎癥環境塑造了更具攻擊性的微生物群,這在連續移植到IL-10基因敲除小鼠中引起了更嚴重的結腸炎;4以上發現支持一種IBD發病機制模型,即宿主炎癥促進了具有攻擊性的常駐細菌的擴張,進而加劇了由腸道炎癥引起的菌群失調;5本研究結果提示,優化的小鼠適應人類微生物群模型可以作為研究人類微生物群驅動的疾病表型的有力工具。湖南菌群移植怎么做