商機詳情 -
武漢多種位點組織芯片應用
多種位點組織芯片產生的數據豐富且復雜,需要采用深度系統的分析方法進行解讀。在數據處理過程中,借助專業的圖像分析軟件,對芯片上每個位點的染色結果進行數字化處理,精確提取目標蛋白表達強度、陽性細胞比例等量化指標。通過統計學方法,對不同位點間的數據進行對比分析,挖掘組織樣本中的共性與差異特征。此外,結合生物信息學技術,將芯片數據與基因表達譜、臨床信息等多維度數據進行整合分析,構建復雜的生物網絡模型,揭示組織樣本中分子間的相互作用關系。這種深度系統的數據分析方式,能夠從海量數據中提煉出有價值的生物學信息,為疾病機制研究、預后評估以及藥物靶點發現等提供有力的數據支持,提升研究成果的科學性和實用性。多重免疫熒光平臺憑借其獨特的酪胺信號放大(TSA)技術,展現出明顯的多重檢測與高靈敏度優勢。武漢多種位點組織芯片應用
多重免疫熒光平臺在實驗資源利用和研究效率提升方面具有明顯好處,為生物醫學研究提供了重要的支持。通過在同一張切片上進行多重檢測,該平臺能夠盡可能地利用有限的組織樣本,減少樣本浪費。這對于珍貴的臨床樣本尤為重要,能夠確保樣本的高效利用。此外,該平臺的高通量檢測能力和多輪染色操作明顯提高了實驗效率,縮短了研究周期。通過減少實驗步驟和試劑用量,多重免疫熒光平臺還降低了實驗成本,使得更多的實驗室能夠承擔大規模的樣本分析工作。這些優點不僅提高了研究效率,還為研究人員提供了更豐富的數據,有助于更系統地理解復雜的生物過程。因此,多重免疫熒光平臺成為生物醫學研究中的重要工具,為高質量的研究結果提供了有力保障。合肥原位雜交平臺組織芯片免疫組化服務的實驗流程環環相扣,每一步都經過精心設計與優化。
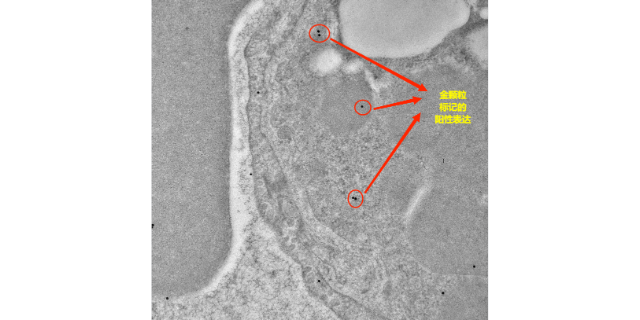
多重免疫熒光平臺憑借其獨特的酪胺信號放大(TSA)技術,展現出明顯的多重檢測與高靈敏度優勢。TSA技術利用辣根過氧化物酶(HRP)催化酪胺自由基與組織抗原周圍的酪氨酸殘基發生共價結合,從而在抗原位點上沉積大量熒光信號。這一過程不僅明顯增強了信號強度,還使得該平臺能夠檢測到低豐度的靶標,這對于研究復雜的生物過程和組織微環境至關重要。與傳統的免疫組化技術相比,多重免疫熒光平臺能夠有效避免熒光信號的串色問題,確保檢測結果的準確性和可靠性。此外,該平臺兼容多種抗體和熒光染料,可在同一組織切片上進行多輪染色,有效提高了實驗效率和數據豐富度。這種多重檢測能力使得研究人員能夠在同一張切片上同時觀察多個標志物的表達和分布,為深入理解細胞間相互作用和信號傳導提供了有力支持。
藥物研發環節,組織芯片大放異彩。在藥物靶點確認階段,將候選靶點相關蛋白的檢測集成于芯片,觀察其在病變與正常組織中的表達差異,精細判斷靶點可行性。進入藥效評估時,用組織芯片呈現藥物作用后細胞的形態學改變,如細胞凋亡增加、增殖受抑的情況,直觀展現藥物療效。像在抗心血管疾病藥物研發中,對心臟、血管組織芯片用藥前后對比,監測心肌細胞肥大改善、血管平滑肌舒張等指標,較大縮短研發周期。同時,還能提前察覺藥物潛在不良反應,通過觀察肝腎組織芯片有無損傷跡象,保障藥物安全性,多方面加速新藥推向市場。多種位點組織芯片產生的數據豐富且復雜,需要采用深度系統的分析方法進行解讀。
組織芯片技術服務配備多種檢測方法和技術。免疫組化是較常用的檢測技術之一,通過抗原 - 抗體特異性結合,利用顯色劑使目標抗原在組織切片上呈現顏色,從而定位和檢測蛋白質的表達。原位雜交技術則用于檢測組織中的核酸序列,可確定特定基因的表達位置和水平。此外,還有熒光原位雜交、熒光定量 PCR 等技術,能夠對組織芯片上的核酸進行定量分析。這些檢測技術相互補充,為研究人員提供了多方面、準確的組織樣本信息,助力深入探究疾病的分子機制。原位雜交技術服務適用于多種樣本類型,在基礎科研與臨床應用中展現出良好的兼容性。武漢多種位點組織芯片應用
組織芯片免疫熒光方案在生物醫學研究和臨床應用中具有廣闊的應用范圍。武漢多種位點組織芯片應用
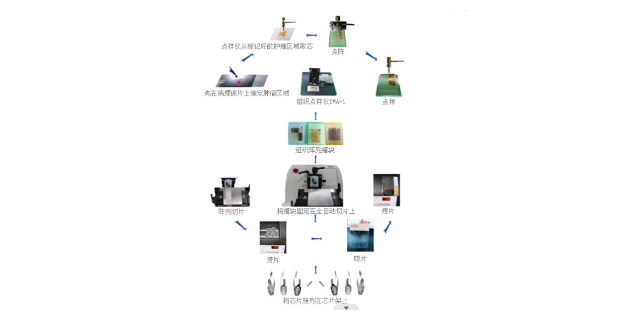
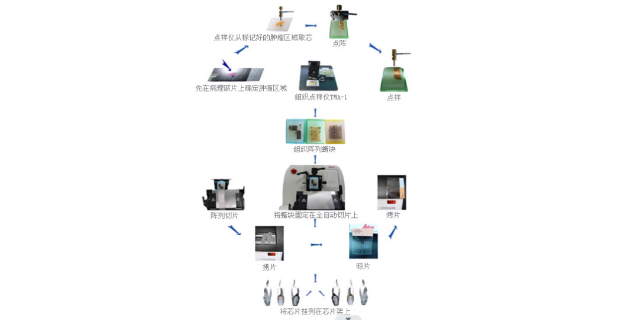
制作組織芯片是一個精細而復雜的過程。首先,要對供體組織進行嚴格篩選和病理診斷,明確其特征和代表性。然后,使用專門的組織芯片制作儀進行操作。通過高精度的打孔針從石蠟包埋的組織塊中取出微小的組織芯,一般直徑在 0.6 - 2mm 之間,這些組織芯會按照預定的陣列設計被精細地放置在空白的受體蠟塊中,排列成整齊的矩陣。制作完成后,進行切片,切片厚度通常為 4 - 5μm,與常規病理切片相似。整個過程需要嚴格控制溫度、濕度和操作的精細度,以保證組織芯片的質量,任何一個環節的失誤都可能影響后續的檢測結果。武漢多種位點組織芯片應用