商機詳情 -
海南肺纖維化模型如何構建
肺纖維化是一種慢性進行性肺部疾病,會導致肺功能性氣體交換功能受損、呼吸衰竭甚至死亡。該病的發***展的起因是多種因素引起的早期肺部炎癥,這些炎癥的長期持續將導致肺內纖維組織沉積,誘發肺纖維化。已有研究表明,肺成纖維細胞的異常激發和分化是致病因素之一,而持續性肺泡損傷和修復不完全也可促進肺纖維化
高濃度氧、石棉等均可以作為誘導劑來引起肺纖維化,其中以博來霉素比較為常用。博萊霉素是一種**藥物,對肺部存在毒性副作用。該藥可以誘導DNA的斷裂與氧化應激反應,從而引起實質炎癥、上皮細胞損傷伴反應性增生、上皮-間充質轉化、成纖維細胞活化并分化為肌成纖維細胞,以及基底膜和肺泡上皮損傷等癥狀。 在肺纖維化模型中,免疫抑制療愈對肺纖維化的進程有一定影響。海南肺纖維化模型如何構建
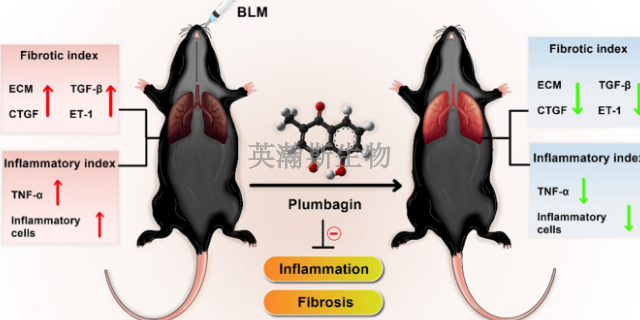
肺纖維化形成***組織。***一旦形成,便是長久性的。基于疾病的不同,可采取如下方式延緩疾病進展,開展預防:特發性肺纖維化的療愈選擇非常有限。盡管研究試驗仍在進行,目前為止沒有證據表明任何藥物可以明顯改善病情。重癥病例單獨可能的療愈選擇是肺移植。某些類型的肺纖維化對皮質類固醇(如潑尼松)及其他免疫抑制藥物產生反應,因此有時會使用這些藥物減緩纖維化過程。免疫系統在多種肺纖維化的發展中發揮著中心作用。使用免疫抑制劑(如皮質類固醇)的目的是減少肺部炎癥和伴隨的瘢痕形成。病情對藥物療愈的反應不盡相同。免疫抑制療愈有效的患者或許并非患有特發性肺纖維化,特發性肺纖維化尚無明確的療愈方法。湖北比較好的肺纖維化模型有哪家科學家通過肺纖維化模型發現了一些與疾病相關的微小RNA。
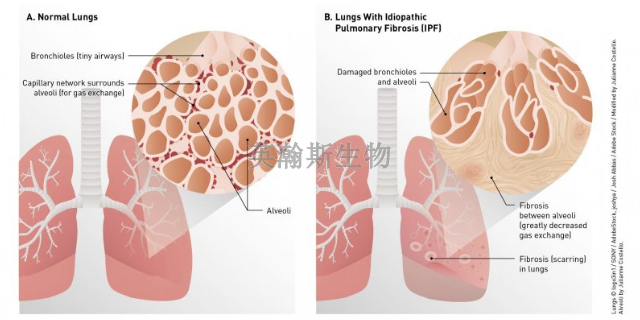
肺間質纖維化的形成是許多慢性肺疾病的共同結局,其病理特點是長期肺部炎癥導致肺泡持續性損傷以及細胞外基質(EcM)的反復破壞、修復和改建。博萊霉素引起的急性肺損傷(ALI)可導致成纖維細胞及肌成纖維細胞的增生,這些增生的細胞可產生大量ECM,比較終導致纖維化的形成。給予博萊霉素后小鼠表現為炎癥反應,早期為急性中性粒細胞浸潤,隨后過渡為淋巴細胞增多的慢性表現,與Izbicki等“的研究結果一致。Tarnell等的研究指出,纖維化模型BALF中中性粒細胞比血液中中性粒細胞產生更多的超氧陰離子。然而這種反應是暫時的,在明顯纖維化發生之前中性粒細胞就已恢復到正常水平,所以這些細胞可能并不直接作用于纖維化的起始。
④諸多肺纖維化動物模型造模方法中以博來霉素誘導的建模方法較為常用,此法可選擇多樣化的給***式、且在使用鼻飼給藥時穩定性較高,造模時相對安全不易產生意外導致小鼠死亡、造模的周期短和建模價格低廉,但此方法的缺點是誘導的纖維化只是間質性纖維化的一般形態而不具有特異性;而在環境因素誘導的建模中,比較推薦的誘導物為二氧化硅,但由于環境因素在造模的過程中對人體損害很大,現已很少使用。⑤文章綜合考慮認為,通過對肺纖維化動物模型的生物因素及非生物因素造模方法進行比較,有助于在動物實驗過程中選擇合適的模型;根據研究者自身的實驗目的及需求,以博來霉素鼻飼誘導建立肺纖維化動物模型是較好的選擇。肺纖維化模型為研究疾病過程中的細胞凋亡和自噬提供了平臺。
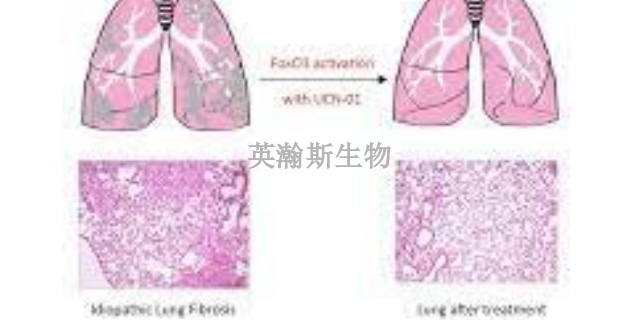
Masson染色、肺組織羥脯氨酸含量、血氣分析等結果可以評估肺纖維化模型是否造模成功。通過Western blot檢測肺組織中E鈣黏素、波形蛋白、α平滑肌肌動蛋白(αsmooth muscle actin,αSMA)等蛋白標記評估肺組織纖維化程度。結果氣道噴霧給藥后,伊文斯蘭染液在肺組織中的分布更為均勻;給藥后各時間點結果顯示,相較于對照組,實驗組大鼠HE及Masson染色提示肺組織中成纖維細胞及膠原含量逐步增多,肺組織羥脯氨酸含量明顯升高(P<005);除28 d組外,其余各組動脈血氧分壓較對照組明顯下降(P<005)。肺纖維化模型可以模擬肺纖維化患者的呼吸功能障礙。山東比較好的肺纖維化模型有哪家
肺纖維化模型為研究肺纖維化與心血管疾病的關系提供了線索。海南肺纖維化模型如何構建
肺纖維化模型在醫學研究中扮演著不可或缺的角色,尤其是在揭示肺纖維化疾病過程中炎癥介質的作用方面。炎癥介質作為調節炎癥反應的關鍵因子,其活性和水平的異常在肺纖維化的發病和發展中起到了重要作用。通過肺纖維化模型,研究人員能夠模擬出肺纖維化的病理過程,并觀察和分析炎癥介質在這一過程中的具體作用。這些模型顯示,炎癥介質在肺纖維化早期會促進炎癥細胞的聚集和活化,進而加劇炎癥反應;而在疾病后期,它們則可能參與纖維化的形成和進展。通過深入研究這些炎癥介質的作用機制,我們不僅能夠更好地理解肺纖維化的發病機制,還能夠為開發新的療愈策略提供重要線索。海南肺纖維化模型如何構建