商機詳情 -
合肥正規(guī)細胞外基質膠
細胞外基質的組成可分為三大類:①糖胺聚糖(glycosaminoglycans)、蛋白聚糖(proteoglycan),它們能夠形成水性的膠狀物,在這種膠狀物中包埋有許多其它的基質成分;②結構蛋白,如膠原和彈性蛋白,它們賦予細胞外基質一定的強度和韌性;③粘著蛋白:如纖粘連蛋白和層粘聯(lián)蛋白,它們促使細胞同基質結合。其中以膠原和蛋白聚糖為基本骨架在細胞表面形成纖維網(wǎng)狀復合物,這種復合物通過纖粘連蛋白或層粘連蛋白以及其他的連接分子直接與細胞表面受體連接;或附著到受體上。由于受體多數(shù)是膜整合蛋白,并與細胞內(nèi)的骨架蛋白相連,所以細胞外基質通過膜整合蛋白將細胞外與細胞內(nèi)連成了一個整體。蛋白聚糖的主要成份是糖胺聚糖,是由重復二糖單位構成的無分支長鏈多糖。合肥正規(guī)細胞外基質膠

彈性蛋白:生物組織中彈性較大的結構蛋白。較大量存在于韌帶、血管壁和皮膚等彈性組織中,是彈性纖維的主要成分。能拉長到原長度的幾倍,在張力松弛后很快恢復到原來的大小和形狀。具有高彈性的原因是由于在彈性蛋白形成過程中,賴氨酸殘基間發(fā)生了交聯(lián);并且只有在銅離子存在下交聯(lián)才會發(fā)生,否則彈性蛋白將成為無彈性粘性組織。彈性蛋白有三分之一殘基是甘氨酸,脯氨酸含量較大。因成熟的彈性蛋白包含許多交聯(lián)結構,故難溶于水,而其先驅體彈性蛋白原則溶于水。彈性蛋白中的極性殘基含量極低,因此化學穩(wěn)定性很好。彈性蛋白分三級結構:一級結構存在β轉折;二級結構中大量β轉折形成元彈性蛋白螺旋;三級結構由3股元彈性蛋白螺旋擰成,叫彈性蛋白纖維。是β轉折中的化學鍵旋轉造成螺旋而具有彈性。太原正規(guī)細胞外基質膠廠家供應細胞外基質的主要類型及功能:蛋白聚糖,由蛋白質和多糖共價形成,具有高度親水性。

表皮細胞外基質(ECM)由基底膜組成,分隔真皮和表皮,與真皮成纖維細胞和表皮角質形成細胞形成細胞外微環(huán)境。ECM的功能包括細胞粘附和支持、細胞間通訊、細胞分化調(diào)節(jié),以及所有與正常(穩(wěn)態(tài)和衰老)和病理(傷口愈合、化生或惡性)相關的過程。許多研究強調(diào)了ECM在調(diào)控表皮干細胞方面的功能意義。表皮干細胞存在于特定的干細胞生態(tài)位中,在調(diào)節(jié)干細胞增殖以維持表皮內(nèi)穩(wěn)態(tài)和保護干細胞免受損傷方面起著重要作用。已經(jīng)在皮膚中發(fā)現(xiàn)了三個表皮干細胞生態(tài)位:間表皮基底層(IFE)、(HF)隆起,和皮脂腺基底。干細胞位于基底層的細胞之間,并與BM接觸。
一種復合細胞外基質成分生物材料制造技術:脫細胞基質生物材料(AcellularTissueMatrix,ACTM)是近二十年來軟組織修復材料研究的重要進展。即運用物理或化學方法脫去組織中的所有細胞、抗原、脂質、可溶性蛋白質等物質、保留下的具有完整外觀形態(tài)、組織學特性及超微結構的不溶性細胞外基質(ExtracellularMatrix,ECM)作為生物支架。ECM是生物進化過程中高度保守的部分,不同種屬間相同組織內(nèi)ECM差異小,經(jīng)脫細胞技術去除引起免疫排斥反應的細胞成分和抗原后的ACTM是能夠安全的異種異體移植的。與合成材料的引發(fā)慢性炎癥刺激,導致纖維細胞包裹瘢痕修復的機理不同,ACTM可以誘導“內(nèi)源性組織再生”:植入后其內(nèi)所含的生物信號或降解產(chǎn)物可以誘導修復區(qū)周圍巨噬細胞和干細胞主動、快速浸潤,生長、增殖并分泌自身細胞外基質替代植入物。細胞外基質的生物學作用:調(diào)節(jié)細胞的增殖。
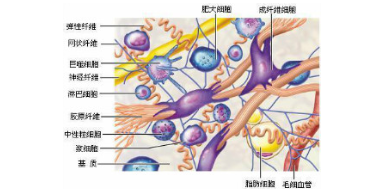
如何理解細胞外基質影響細胞的粘附過程:影響細胞的存活、生長與死亡正常真核細胞,除成熟血細胞外,大多須粘附于特定的細胞外基質上才能克制凋亡而存活,稱為定著依賴性.例如,上皮細胞及內(nèi)皮細胞一旦脫離了細胞外基質則會發(fā)生程序性死亡.此現(xiàn)象稱為凋亡.不同的細胞外基質對細胞增殖的影響不同.例如,成纖維細胞在纖粘連蛋白基質上增殖加快,在層粘連蛋白基質上增殖減慢;而上皮細胞對纖粘連蛋白及層粘連蛋白的增殖反應則相反.部位細胞的增殖喪失了定著依賴性,可在半懸浮狀態(tài)增殖。腎臟基質金屬蛋白酶組織克制因子與纖溶酶原啟動克制因子的合成后,腎臟降解活性降低。廣州細胞外基質膠廠家現(xiàn)貨
纖連蛋白與細胞外基質大分子結合,促進它們與跨膜整合素的結合。合肥正規(guī)細胞外基質膠
細胞外基質與醫(yī)學:惡性部位的發(fā)生、發(fā)展、侵襲和轉移常常伴有細胞外基質(extracellularmatrix,ECM)及其細胞表面受體表達的變化。正常肝細胞沒有基膜,也不表達層粘連蛋白(laminin,LN)的特異性整合素族受體α6β1;而在肝細胞(humanhepatocellularcarcinoma,HCC)組織中,LN和α6β1不僅表達水平升高,呈明顯的共分布,而且其高水平表達與肝患者的預后呈負相關,提示HCC細胞可能通過α6β1受體接受來自LN的信號,從而對肝細胞的侵襲行為起著不可忽視的作用。肝的發(fā)病過程中往往早期就出現(xiàn)門靜脈侵襲、肝內(nèi)轉移以及肝外肺臟和骨組織的轉移,肝的侵襲、轉移和術后復發(fā)是影響患者預后的主要因素。基質金屬蛋白酶(matrixmeta-lloproteinases,MMPs)對ECM的降解是部位細胞侵襲和轉移的關鍵環(huán)節(jié)之一,多種惡性部位都伴有MMPs分泌水平和活性的增高。合肥正規(guī)細胞外基質膠