商機(jī)詳情 -
江西值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
新藥往往需要臨床前動(dòng)物實(shí)驗(yàn),從設(shè)計(jì)到上市通常需要10-15年的時(shí)間,經(jīng)歷漫長的研發(fā)過程和層層考驗(yàn),同時(shí)需要大量的資本投入。藥物通過發(fā)現(xiàn)篩選、臨床前研究、臨床試驗(yàn)、新藥NMPA/FDA上市申報(bào)等環(huán)節(jié),比較終成為穩(wěn)定、安全、有效的藥品,惠及人類健康。其中的每個(gè)研究階段都至關(guān)重要,特別是臨床前藥物研究獲得的結(jié)果對(duì)藥物進(jìn)入臨床提供關(guān)鍵的數(shù)據(jù)指導(dǎo),為優(yōu)化臨床開發(fā)計(jì)劃提供有力的數(shù)據(jù)基礎(chǔ)。臨床前動(dòng)物實(shí)驗(yàn)是其中非常重要的一環(huán),起到承上啟下的作用。生物藥臨床前動(dòng)物實(shí)驗(yàn)機(jī)構(gòu);江西值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
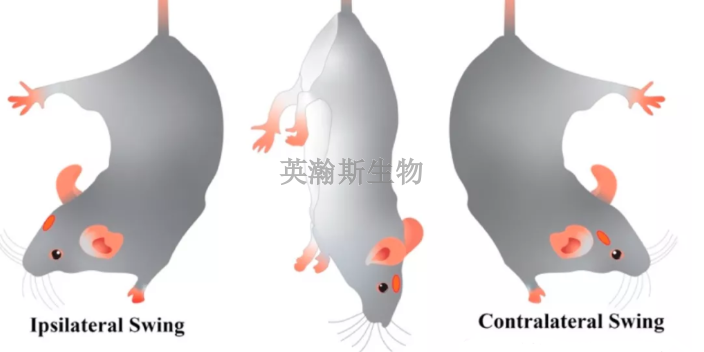
臨床前動(dòng)物實(shí)驗(yàn)方案盡可能模擬臨床設(shè)計(jì)和使用。應(yīng)當(dāng)確認(rèn)在輸送、植入或使用器械中的所有步驟,并制定每一個(gè)步驟的可接受標(biāo)準(zhǔn)。建議對(duì)每個(gè)驗(yàn)收標(biāo)準(zhǔn)應(yīng)用半客觀的評(píng)定量化表(例如李克特量表,Likertscale)。如果器械與輔助設(shè)備一同輸送或使用,則可接受標(biāo)準(zhǔn)應(yīng)包含評(píng)估系統(tǒng)相容性的要素。評(píng)級(jí)標(biāo)準(zhǔn)應(yīng)當(dāng)囊括從器械準(zhǔn)備到放置或使用乃至取回和重新放置過程中的所有步驟。如果器械通過手術(shù)放置,則應(yīng)描述器械從進(jìn)入體壁到比較終器械操作期間的所有步驟。江蘇專注臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液蒙锼幣R床前動(dòng)物實(shí)驗(yàn)多少錢?
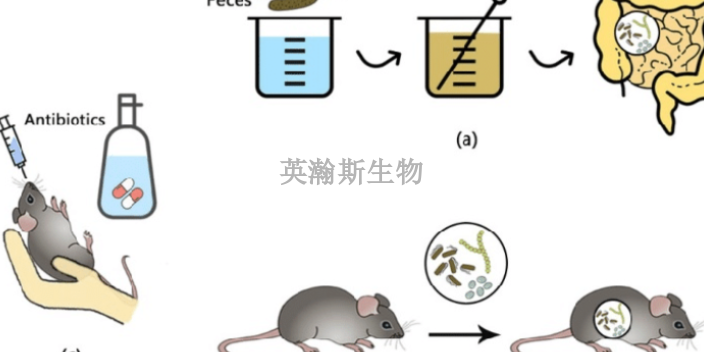
臨床前動(dòng)物實(shí)驗(yàn)附屬器械和設(shè)備風(fēng)險(xiǎn):某些受試品常常與某些特定的附屬裝置或部件結(jié)合使用。當(dāng)試驗(yàn)器械必須與附件一同使用時(shí),這些附件有時(shí)被描述為實(shí)驗(yàn)系統(tǒng)的一部分。在這種情況下,應(yīng)考慮臨床前動(dòng)物實(shí)驗(yàn)研究中使用的任何附屬器械是否與試驗(yàn)器械完全分離,或者附屬器械是否將與受試品一起上市銷售;以及器械的**終標(biāo)簽是否包含附屬器械選擇或使用的說明。建議在實(shí)驗(yàn)動(dòng)物中評(píng)價(jià)/測試醫(yī)療器械的方法和材料應(yīng)與使用在現(xiàn)代獸醫(yī)和醫(yī)院中的方法類似。監(jiān)測和干預(yù)策略應(yīng)基于獸醫(yī)和專業(yè)人員以往的經(jīng)驗(yàn)。一旦確定動(dòng)物實(shí)驗(yàn)研究中可以解決的失敗模式和影響因素,則應(yīng)制定動(dòng)物實(shí)驗(yàn)方案以解決每項(xiàng)已識(shí)別的風(fēng)險(xiǎn),并規(guī)定監(jiān)測、干預(yù)措施和結(jié)果評(píng)估的頻次和類型。
為申請(qǐng)藥品注冊(cè)而進(jìn)行的藥物臨床前研究,包括藥物合成工藝、提取方法、理化性質(zhì)及純度、劑型選擇、***篩選、制備工藝、檢驗(yàn)方法、質(zhì)量指標(biāo)、穩(wěn)定***理、毒理、動(dòng)物藥代動(dòng)力學(xué)等。中藥制劑還包括原藥材的來源、加工及炮制等,生物制品還包括菌毒種、細(xì)胞株、生物組織等起始材料的來源、質(zhì)量標(biāo)準(zhǔn)、保存條件、生物學(xué)特征、遺傳穩(wěn)定性及免疫學(xué)的研究等。根據(jù)藥品注冊(cè)申報(bào)資料要求,臨床前研究可概括為3方面:(1)文獻(xiàn)研究:包括藥品名稱和命名依據(jù),立題目的與依據(jù)。(2)藥學(xué)研究:原料藥工藝研究,制劑***及工藝研究,確證化學(xué)結(jié)構(gòu)或組份的試驗(yàn),藥品質(zhì)量試驗(yàn),藥品標(biāo)準(zhǔn)起草及說明,樣品檢驗(yàn),輔料,穩(wěn)定性試驗(yàn)、包裝材料和容器有關(guān)試驗(yàn)等。(3)藥理毒理研究:一般藥理試驗(yàn),主要藥效學(xué)試驗(yàn)、急性毒性試驗(yàn),長期毒性試驗(yàn),過敏性、溶血性和局部刺激性試驗(yàn)、致突變?cè)囼?yàn)、生殖毒性試驗(yàn)、致*毒性試驗(yàn),依賴性試驗(yàn),動(dòng)物藥代動(dòng)力學(xué)試驗(yàn)等。臨床前藥物安全性評(píng)價(jià)(DSE)是藥物臨床前研究的**內(nèi)容。藥物的安全性評(píng)價(jià)研究必須執(zhí)行《藥物非臨床研究質(zhì)量管理規(guī)范》(GLP)。化學(xué)藥臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液茫?/p>
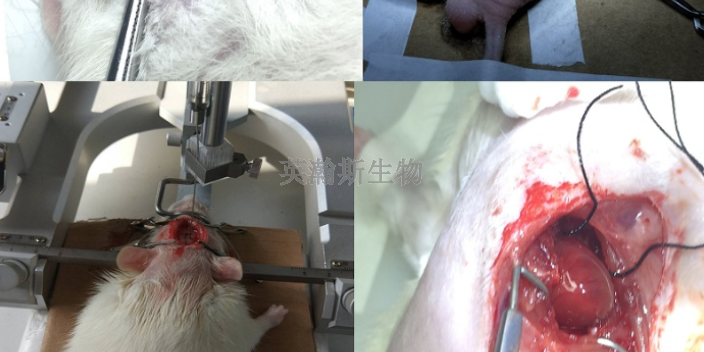
我國醫(yī)療器械臨床前安全性評(píng)價(jià)還沒有實(shí)施GLP管理,但要求開展醫(yī)療器械生物學(xué)評(píng)價(jià)試驗(yàn)機(jī)構(gòu)需要具備中國合格評(píng)定國家認(rèn)可委員會(huì)(ChinaNationalAccreditationServiceforConformityAssessment,CNAS)及中國計(jì)量認(rèn)證(ChinaMetrologyAccreditation,CMA)認(rèn)可的實(shí)驗(yàn)室資質(zhì),而對(duì)開展臨床前動(dòng)物實(shí)驗(yàn)研究還沒有明確的資質(zhì)要求。GLP管理與CNAS認(rèn)證體系雖然是兩個(gè)不同的質(zhì)量管理體系,但基本內(nèi)容有很多的相同性和相似性。如果參照我國相關(guān)醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究指導(dǎo)原則和國家或行業(yè)標(biāo)準(zhǔn),在具備CNAS及CMA認(rèn)可資質(zhì)的實(shí)驗(yàn)室質(zhì)量管理體系下開展醫(yī)療器械臨床前動(dòng)物實(shí)驗(yàn)研究,可以基本滿足臨床前動(dòng)物實(shí)驗(yàn)研究質(zhì)量管理要求。化學(xué)藥臨床前動(dòng)物實(shí)驗(yàn)中心;重慶比較好的臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
中成藥臨床前動(dòng)物實(shí)驗(yàn)研究;江西值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
全國外科植入物與矯形器械標(biāo)準(zhǔn)化技術(shù)委員會(huì)組織工程醫(yī)療器械產(chǎn)品分技術(shù)委員會(huì)(SAC/TC110/SC3)組織制定了幾項(xiàng)臨床前動(dòng)物實(shí)驗(yàn)研究相關(guān)的標(biāo)準(zhǔn),即YY/T0606.10-2008“組織工程醫(yī)療產(chǎn)品第10部分:修復(fù)或再生關(guān)節(jié)軟骨的植入物體內(nèi)評(píng)價(jià)指南”、YY/T1575-2017“組織工程醫(yī)療器械產(chǎn)品修復(fù)和替代骨組織植入物骨形成活性的評(píng)價(jià)指南”、YY/T1598-2018“組織工程醫(yī)療器械產(chǎn)品骨用于脊柱融合的外科植入物骨修復(fù)或再生評(píng)價(jià)試驗(yàn)指南”、YY/T1636-2018“組織工程醫(yī)療器械產(chǎn)品體內(nèi)臨界尺寸骨缺損的臨床前評(píng)價(jià)指南”。這些標(biāo)準(zhǔn)針對(duì)軟骨和骨植入物的臨床前動(dòng)物實(shí)驗(yàn)研究,給出了實(shí)驗(yàn)動(dòng)物的選擇、觀察周期及觀察終點(diǎn)指標(biāo)的確定等具體要求和指導(dǎo)。江西值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
擴(kuò)展資料
臨床前動(dòng)物實(shí)驗(yàn)熱門關(guān)鍵詞
臨床前動(dòng)物實(shí)驗(yàn)企業(yè)商機(jī)
- . 江西臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?
- . 陜西專注臨床前動(dòng)物實(shí)驗(yàn)多少錢
- . 四川推薦的臨床前動(dòng)物實(shí)驗(yàn)公司
- . 陜西有什么臨床前動(dòng)物實(shí)驗(yàn)外包
- . 甘肅靠譜臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?
- . 云南值得信賴臨床前動(dòng)物實(shí)驗(yàn)
- . 內(nèi)蒙古比較好的臨床前動(dòng)物實(shí)驗(yàn)外包
- . 陜西個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 江西值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
- . 云南個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)公司
臨床前動(dòng)物實(shí)驗(yàn)行業(yè)新聞
- . 專業(yè)臨床前動(dòng)物實(shí)驗(yàn)檢測
- . 貴州高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)是什么
- . 廣東專業(yè)臨床前動(dòng)物實(shí)驗(yàn)指標(biāo)
- . 河北什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 河南值得信賴臨床前動(dòng)物實(shí)驗(yàn)研究
- . 生物藥臨床前動(dòng)物實(shí)驗(yàn)是什么
- . 化妝品臨床前動(dòng)物實(shí)驗(yàn)指導(dǎo)原則
- . 黑龍江個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)外包
- . 吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 西藏有什么臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
-
靠譜臨床前動(dòng)物實(shí)驗(yàn)外包
-
云南有什么臨床前動(dòng)物實(shí)驗(yàn)是什么
-
寧夏靠譜臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?/p>
-
云南個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)是什么
-
四川值得信賴臨床前動(dòng)物實(shí)驗(yàn)研究
-
內(nèi)蒙古有什么臨床前動(dòng)物實(shí)驗(yàn)外包
-
浙江高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
-
江蘇值得信賴臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
-
黑龍江值得信賴臨床前動(dòng)物實(shí)驗(yàn)
-
陜西有什么臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)