商機詳情 -
天津推薦的藥物安全性評價多少錢
對于動物模型的使用需要考慮到其與人類生理學的差異,因此,越來越多的研究也在探索使用體外模型和計算機模擬技術來替代動物實驗,以提高評價的準確性和可靠性。此外,計算機輔助技術在藥物安全性評價中也發揮著重要作用。通過使用計算機模擬和預測技術,研究者可以對藥物的分子結構、代謝途徑和與生物分子的相互作用進行建模和分析,從而更準確地預測藥物的毒性和不良反應。總的來說,藥物安全性評價技術和方法的研究涉及到多個學科領域,包括藥理學、毒理學、生物化學、計算機科學等,其重要性和必要性不言而喻。隨著科學技術的不斷進步和完善,我們有理由相信,藥物安全性評價領域將會迎來更多新的突破和創新,為人類健康事業作出更大的貢獻。英瀚斯藥物安全性評價研究 遵循國內GLP管理規范及國外相關法規要求。天津推薦的藥物安全性評價多少錢
藥物安全性評價,藥學研究的風險控制與階段性要求創新藥的藥學研究主要是為了滿足不同階段臨床試驗需要,IND階段藥學研究應首先能進行藥物安全性評價。目前,一般認為,對于創新藥可能引起臨床安全性的主要風險包括:產品未知或不純組分、化學結構含有或潛在毒性成分、穩定性差、雜質未充分確定等[]。這其中涉及單抗產品的主要風險為,細胞庫未充分檢定、動物源性成分生物安全性風險、生產工藝不穩定造成生物活性改變等。因此,藥學研究若存在上述(不限于)影響臨床用藥安全性的重大缺陷,申請人必須在開展臨床試驗前予以解決。天津推薦的藥物安全性評價多少錢英瀚斯生物專業為客戶提供藥物安全性評價!
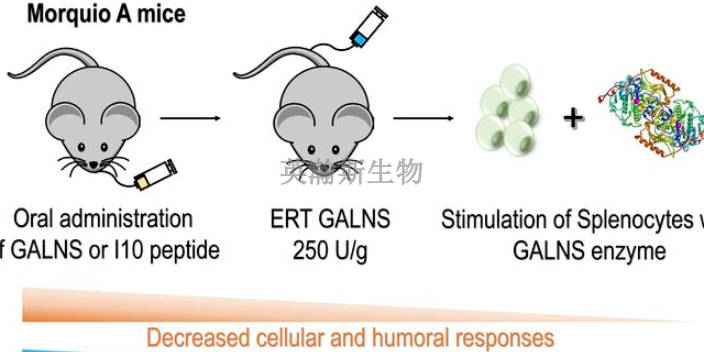
在藥物安全性評價方面,體外實驗技術是不可或缺的一部分。體外實驗可以通過使用細胞培養、細胞系、組織切片等模型來模擬藥物在體內的作用和代謝過程,從而評估藥物對細胞和組織的毒性和影響。此外,體外實驗還包括了對藥物在生物體外環境中的化學性質和穩定性的評估,這些信息對于預測藥物在體內的行為至關重要。另一方面,體內實驗技術也是藥物安全性評價的重要組成部分。體內實驗通過使用動物模型或人體志愿者來評估藥物在整體生物系統中的行為和效果。這種方法可以更普遍地了解藥物的代謝途徑、藥效學特性以及潛在的毒性和不良反應。
長期以來,我國的生物制藥申報以“生物類似藥”為主,藥物評價關注于候選藥與原研藥之間質量比對研究的“相似性”,藥效毒理比較研究的“橋接性”、臨床試驗的“非劣性”和臨床價值的“可接受性”。因此,抗體生物類似藥在申請IND前應基本確定生產工藝,并進行充分的結構確證與質量研究。而創新型抗體藥物研發進程具有“創試性”(臨床試驗存在較大的失敗風險)、“階段性”(藥學研究可分階段展開)和“漸進性”(臨床期間通常發生工藝變更)的特征,其評價關注點應區別于傳統生物類似藥,藥學研究內容可按照臨床試驗進展分階段進行要求,重點關注于影響臨床藥物安全性評價問題。新藥研發的必需組成部分是藥物安全性評價。

藥物安全性評價的發展史,就不得不提一下沙利度胺(反應停)作為藥物安全性評價的典型反面教材。在該藥上市的短短幾年,全球出生了10000余名短肢畸形的嬰兒(海豚兒)。而FDA審查員凱爾西女士在審查該藥物的上市申請時,在一項研究中看到沙利度胺有神經系統副作用,堅持要求廠商補充試驗資料。正是這樣的堅持,使得美國避免了這場悲劇,凱爾西女士也因此獲得了肯尼迪親自授予的“杰出聯邦公民總統獎”。在凱爾西女士的大力推動下,美國通過了《柯弗瓦哈里斯修正案》。英瀚斯藥物安全性評價,特殊毒性試驗:溶血、過敏、刺激性試驗等。青海藥物安全性評價檢測
藥物安全性評價的指標包括哪些內容?天津推薦的藥物安全性評價多少錢
藥物安全性是導致藥物研發失敗的重要因素,也是上市藥物退市的主要原因。傳統上藥物的毒性測試及安全性評價一般在臨床前階段的動物試驗中完成,一旦發現藥物嚴重的毒性反應而導致研發失敗將造成巨大的經濟損失。在藥物研發的早期階段進行離子通道、細胞水平上的藥物毒性測試將明顯降低后期藥物研發失敗的機率,從而降低研發成本。我們可以為客戶提供體外早期毒性篩選到體內早期毒性評價的完整策略,幫助我們的客戶在藥物研發的早期發現研發化合物的毒性作用。單次及反復給藥的毒性篩選實驗:個性化設計、快速、高效并準確的預測體內藥物毒性及毒靶;可在小動物上開展。天津推薦的藥物安全性評價多少錢