商機詳情 -
上海生物試劑進出口清關手續
生物試劑種類繁多,常見有化學試劑類,如各種緩沖液、培養基成分等,其進出口相對常規,但也要符合化學試劑相關法規,對純度、雜質限量有要求。生物活性試劑,像抗體、重組蛋白等,具有生物活性,保存和運輸條件苛刻,進出口時對冷鏈要求嚴格,且需提供詳細產品活性數據與質量證明。診斷試劑作為特殊一類,用于疾病診斷,各國對其監管更為嚴格,進口時要通過復雜注冊審批程序,確保產品準確性、特異性和穩定性。此外,還有細胞類生物試劑,如細胞株、干細胞等,不運輸需特殊條件維持細胞活性,進出口還涉及生物安全評估,防止外來物種入侵和生物安全風險。不同類型生物試劑進出口特點各異,企業需針對性應對。生物試劑進口需關注目的國對生物試劑行業的扶持政策。上海生物試劑進出口清關手續

出口生物試劑的企業需滿足多方面資質條件。首先,企業要完成對外貿易經營者備案登記,具備合法出口經營權。若生產出口藥品類生物試劑,必須持有有效的藥品生產許可證,且生產車間符合 GMP 要求,保證產品質量穩定可靠。對于醫療器械類生物試劑出口,企業需依據產品風險等級,持有相應的醫療器械生產許可證或完成生產備案。此外,企業應建立完善的質量管理體系,配備熟悉出口法規、產品技術以及國際市場規則的專業團隊,以確保出口業務順利開展并符合各國監管要求。杭州生物試劑進出口審批備案代辦生物試劑進口需關注目的國對生物試劑銷售渠道的限制。
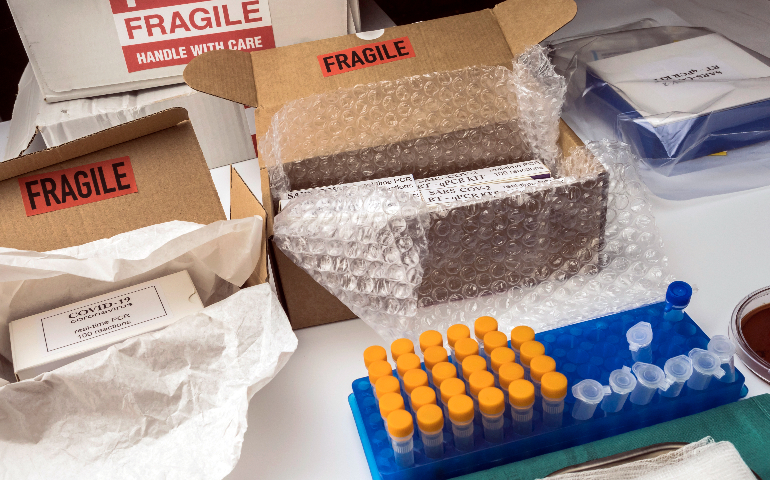
高效的供應鏈管理對生物試劑進出口至關重要。從采購環節開始,企業要與可靠的原材料供應商建立長期穩定合作關系,確保原材料質量穩定且供應及時。例如,生產抗體試劑所需的動物血清,需從符合質量標準的供應商處采購。倉儲管理方面,由于生物試劑特性各異,需分類存儲。對溫度敏感試劑要存放在專業冷鏈倉庫,嚴格控制溫度、濕度等環境參數。運輸過程中,構建多式聯運體系,結合公路、鐵路、航空運輸優勢,實現快速、安全運輸。同時,運用供應鏈管理系統,實時監控貨物運輸狀態、庫存水平等信息,以便及時調整生產、運輸和銷售計劃。通過優化供應鏈管理,降低成本,提高生物試劑進出口效率,保障產品質量與供應穩定性。
生物試劑進出口行業存在多種合作模式。一種是企業間的戰略聯盟,例如國內生物試劑生產企業與國外銷售渠道商建立長期合作關系,生產企業專注于產品研發和生產,利用對方成熟的銷售網絡將生物試劑推向國際市場,實現優勢互補。另一種是產學研合作模式,高校或科研機構與生物試劑企業合作,科研機構提供前沿技術和研究成果,企業負責將其轉化為實際產品并推向市場,在生物試劑進出口業務中,這種合作模式有助于提升產品技術含量和市場競爭力。此外,還有行業協會組織的合作平臺,通過舉辦展會、研討會等活動,促進生物試劑進出口企業之間的交流與合作,共享信息、資源,共同應對行業面臨的問題和挑戰,推動整個行業的協同發展。生物試劑進口需提前規劃好目的國境內的配送方案。
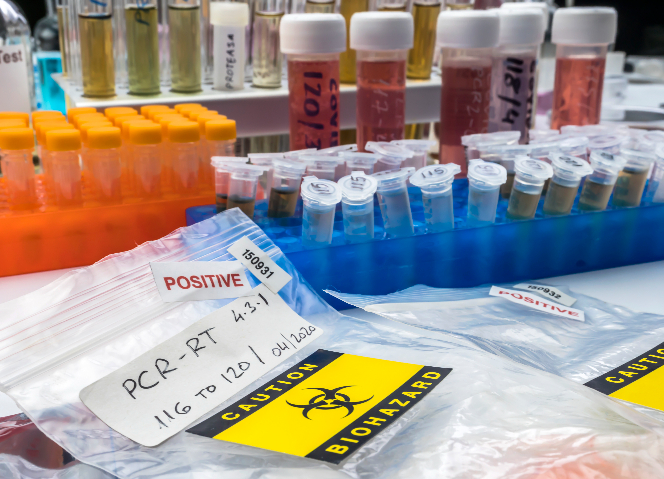
技術創新是生物試劑進出口發展的重心驅動力。在研發環節,基因編輯技術如 CRISPR-Cas9 的突破,催生了一系列新型基因編輯生物試劑,這些試劑在科研和基因醫療領域需求大增,推動了相關試劑的進出口。例如,國外先進企業研發的高精細 CRISPR 基因編輯試劑盒,憑借技術優勢易售全球,國內企業也積極引進并進行本地化生產與改進,促進了該類試劑的進出口貿易。納米技術應用于生物試劑,開發出納米級診斷試劑、藥物載體試劑等,提升了試劑性能,拓展了應用范圍,打開了新的市場需求。此外,生物信息學技術助力生物試劑研發數據處理與分析,加速新型試劑研發進程,研發成果轉化為產品后推動生物試劑進出口業務邁向更高技術水平,為企業帶來競爭優勢。生物試劑進口需提前與目的國收貨人確認接收細節。杭州生物試劑進出口審批備案代辦
出口生物試劑前,要明確進口國對包裝標識的具體規范要求。上海生物試劑進出口清關手續
進出口的生物試劑必須符合目標市場的質量與安全標準。在出口環節,產品要多方面滿足進口國法規及相關國際標準。以出口歐盟的生物試劑為例,其必須符合歐盟指令與協調標準,通過 CE 認證,該認證涵蓋產品安全性、健康影響、環保等多方面評估,只有順利通過認證機構檢測與審核,獲得認證證書,產品才能在歐盟市場流通。出口美國則要符合美國食品藥品監督管理局(FDA)要求并完成相應注冊程序,如醫療器械類生物試劑可能需進行 510 (k) 申請或上市前批準(PMA)等。進口生物試劑時,需確保其符合我國藥品、醫療器械等相關法規,例如藥品類生物試劑要符合我國藥品注冊標準,從藥品的成分、純度到穩定性等各方面都有細致規定;醫療器械類生物試劑要通過國內注冊或備案,產品的研發、生產、質量控制等環節都要達到對應規范,否則產品將無法順利通關,更無法進入市場銷售,還可能面臨召回、處罰等風險。上海生物試劑進出口清關手續